(USS/2015-2) A denominação do ácido de Arrhenius tem origem no século XIX, quando o cientista Svante Arrhenius definiu ácidos como “substâncias que em solução aquosa se ionizam, produzindo como cátion apenas o íon H+ ”.
Observe a tabela abaixo, que apresenta os compostos disponíveis para a realização de um experimento no
qual é necessário um ácido de Arrhenius:
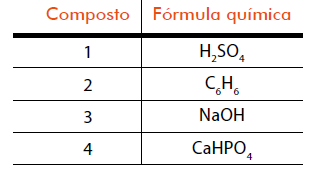
Dentre esses compostos, aquele classificado como ácido de Arrhenius está indicado pelo seguinte número:
A) 1
B) 2
C) 3
D) 4
RESOLUÇÃO:
Como citado no enunciado, ácido de Arrhenius é qualquer composto que libera apenas H+ como cátion.
Dentre as opções apresentadas, o H2SO4 é um ácido de Arrhenius. Na presença de água, o H2SO4 (ácido sulfúrico) se ioniza conforme a equação:

O composto 2 é um hidrocarboneto (benzeno); 3 é um hidróxido (hidróxido de sódio = soda cáustica) e o composto 4 é um sal ácido (hidrogenofosfato de cálcio).
Resp.: A

VEJA TAMBÉM:
– Questão resolvida sobre conceitos de ácidos e bases, da Faculdade de Medicina de Petrópolis
– Questão resolvida sobre ácidos e bases de Brönsted-Lowry, da Unifeso 2021-2
Anúncio. Role para continuar lendo.


